Diferencia entre electrófilo y nucleófilo
- 4930
- 1278
- Carmen Arreola
Electrófilo y los nucleófilos son los dos conceptos importantes en química orgánica que ayudan a describir las reacciones químicas entre los aceptores de electrones y los donantes. Estos dos términos fueron introducidos en 1933 por Christopher Kelk Ingold y sirvieron como reemplazos para los términos catpoides y anionioides que fueron introducidos en 1925 por un.J. Lapworth.
Desde entonces, se realizaron estudios extensos para comprender los diferentes entre electrófilos y nucleófilos. Este artículo desmitifica la diferencia entre estos dos conceptos. En pocas palabras, un nucleófilo es un donante de electrones, mientras que un electrofilo es un aceptador de electrones.
¿Qué es un electrofilo??
Para descomponer el término, la palabra "electro" es de electrones y la palabra latina "file" se refiere a "amor". En términos simples, significa amante de los electrones. Es un reactivo que se caracteriza con una baja densidad de electrones en su carcasa de cenefa y, por lo tanto, reacciona con una molécula, ión o átomo de alta densidad para formar un enlace covalente. El ion de hidrógeno en los ácidos y la metil-carbocation son ejemplos de sustancias electrofílicas. Son deficientes en electrones.
Un electrofilo se detecta fácilmente por una carga positiva o una carga neutral con orbitales vacíos (no satisface la regla del octeto). Los electrones se mueven de un área de alta densidad a la que con baja densidad y, a diferencia de las cargas, se atraen entre sí. Esta teoría explica la atracción de electrones por los átomos electrófilos deficientes en electrones, moléculas o iones. Por definición, un electrofilo se llama indistintamente un ácido de Lewis, ya que acepta electrones en línea con la definición del ácido.
La reacción y los compuestos a continuación muestran los ejemplos de electrofilos:

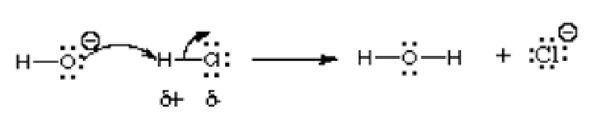
En esta reacción, el ion hidróxido está reaccionando con cloruro de hidrógeno; Así, un ácido está reaccionando con una base. Como lo indica la flecha, el átomo de oxígeno más electronegativo dona electrones al átomo de hidrógeno deficiente en electrones. Comparte un par solitario al átomo de hidrógeno que tiene una carga positiva en el cloruro de hidrógeno compuesto porque es más electronegativo que el hidrógeno. Esta reacción es fundamental de muchas reacciones de química orgánica, particularmente las reacciones de la base de Lewis ácido y Lewis. Otros ejemplos se representan en la siguiente imagen:
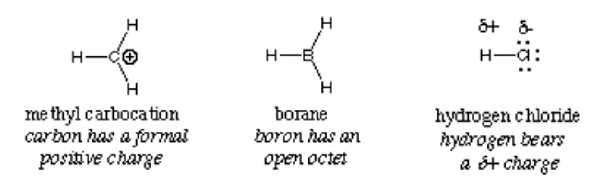
En general, un electrofilo se identifica mediante una carga positiva parcial como en el cloruro de hidrógeno, una carga positiva formal como en la carbocatión metílica o orbitales vacantes. Las moléculas neutras polarizadas, como los haluros de acilo, los compuestos carbonilo y los haluros de alquilo, son ejemplos típicos de electrofilos.
Importante: El ion hidronio, aunque tiene una carga positiva, no califica para clasificarse como un electrofilo debido a los orbitales vacantes completos en su carcasa externa. Produce iones de hidrógeno y agua. Lo mismo se aplica al ion amonio; no tiene orbitales vacantes que puedan atraer electrones. Como resultado, no es un electrofilo.
¿Qué es un nucleófilo??
El término se descompone en la palabra "nuceo" que se refiere al núcleo y la palabra latina "file" que significa amor. Simplemente significa amor a núcleo. Los nucleófilos son ricos en electrones y, como así, donan pares de electrones a electrofilos para formar enlaces covalentes en reacciones químicas. Estas sustancias se notan mejor con pares solitarios, enlaces PI y cargas negativas. Los iones de amoníaco, yoduro e hidróxido son ejemplos de sustancias nucleófilas.
Por definición, un nucleófilo se llama intercambiable la base de Lewis porque todos donan electrones y aceptan protones. La siguiente imagen muestra los ejemplos de nucleófilos:
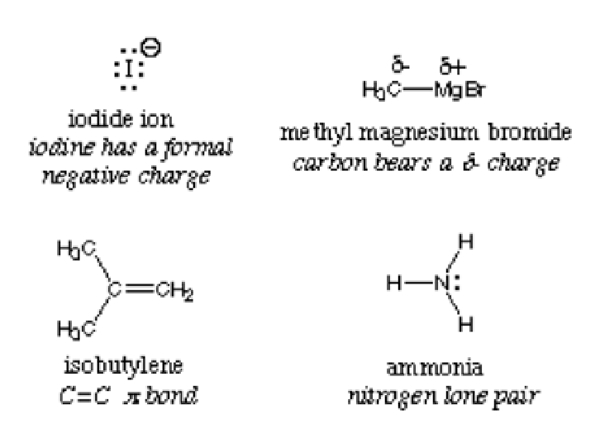
El centro nucleofílico en un compuesto se detecta con el átomo más electronegativo. Considere el amoníaco NH3; El nitrógeno es más electronegativo y, por lo tanto, atrae electrones al centro. El compuesto tiene alta densidad de electrones y, al reaccionar con un electrofilo, digamos agua, dona electrones. H2O puede actuar tanto como el electrofilo como el nucleófilo dependiendo del compuesto o molécula que reaccione con.
Considere la imagen a continuación:
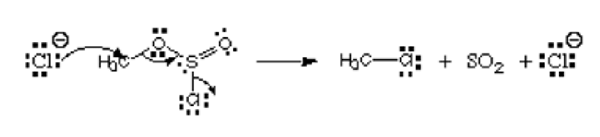
De la imagen, el primer átomo, el ion cloruro está donando su par solitario al carbono para formar un enlace covalente. Tiene la carga negativa y dona electrones, por lo que se considera el nucleófilo. Ese átomo de cloro que está dejando el éster de clorosulfito se llama grupo de salida. No es un electrofilo o un nucleófilo.
Diferencia clave entre electrófilo y nucleófilo
Definición de electrófilo y nucleófilo
Un electrofilo es un ácido de Lewis que acepta electrones de un átomo rico en electrones, iones o moléculas. Al aceptar electrones, forma un enlace covalente. Este reactivo a menudo identificado por carga positiva parcial, carga positiva formal o un átomo neutro, ion o molécula que no satisface la regla del octeto. Un nucleófilo, por otro lado, es un átomo, ion o molécula que tiene una alta densidad de electrones. Dona un par solitario al electrofilo para formar un enlace covalente. Se identifica por cargas positivas y electrones libres en su orbital.
Reacciones químicas de electrófilo y nucleófilo
Un nucleófilo está involucrado en la sustitución y adición nucleofílica, mientras que un electrofilo está involucrado en una sustitución y adición electrofílica.
Identidad de carga en electrófilo y nucleófilo
Un electrofilo puede cargarse neutral o positivamente, mientras que el nucleófilo puede cargarse neutral o negativamente. Un electrofilo acepta electrones, por lo tanto, se conoce como el ácido de Lewis, mientras que un nucleófilo dona electrones, por lo tanto, se conoce como la base de Lewis.
Versos electrófilos Nucleófilo: tabla de comparación

Resumen de los versos electrófilos nucleófilos
- Un electrofilo es un átomo deficiente en electrones, ion o molécula, mientras que el nucleófilo es un átomo rico en electrones, una molécula o ion
- Un electrofilo se puede cargar positiva o neutralmente mientras que el nucleófilo puede cargarse negativamente o neutralmente
- Un electrofilo se llama ácido de Lewis y el nucleófilo se llama base de Lewis
- Un electrofilo acepta electrones y dona protones, mientras que un nucleófilo dona electrones y acepta protones.

