Diferencia entre cetona y éster
- 3923
- 1191
- Maricarmen Moya
Una cetona tiene una estructura molecular que incluye un carbonilo unido a los carbonos, mientras que un éster tiene una estructura molecular en la que un carbonilo está unido a un grupo alcoxi.

Que es la cetona?
Definición:
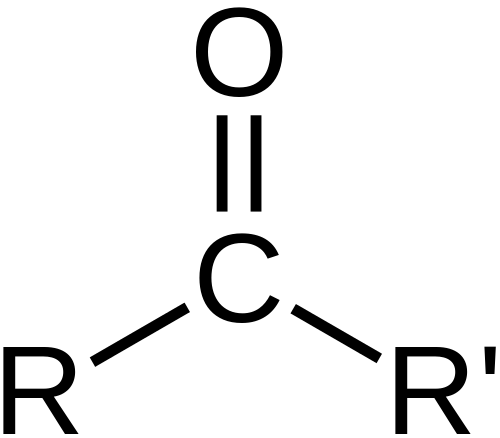
Una cetona es una molécula en la que un átomo de carbono se une covalentemente a un átomo de oxígeno para hacer un grupo de carbonilo y los carbonos están unidos a este carbonilo.
Propiedades:
Las cetonas son moléculas que tienen una alta reactividad y pueden reaccionar fácilmente con otras sustancias. Esto se debe a la naturaleza muy polar del grupo carbonilo que a su vez le da a la molécula una carga positiva parcial. Esto significa que otras sustancias a menudo se sienten atraídas por la molécula con la que luego reaccionan fácilmente. De hecho, la adición nucleofílica y las reacciones de oxidación y reducción son comunes.
Formación:
Hay varias formas en que se puede formar un cetón. Se pueden oxidar muchos alcoholes e hidrocarburos para formar cetonas. Las moléculas llamadas alquynes se pueden modificar por hidratación para formar moléculas de cetona.
Ejemplos y usos:
Hay muchos ejemplos de cetonas que incluyen acetona, feniletanona y propanona. Las cetonas forman la base para la producción de muchos productos útiles en la industria. Por ejemplo, a menudo se usan para hacer varios solventes como la acetona que se usa ampliamente como removedor de esmalte debido a sus propiedades como un excelente solvente. Las cetonas también se pueden usar para desnudar pinturas y lacas e incluso para hacer explosivos y a menudo se usan en la industria de bronceado.
Ocurrencia en la naturaleza:
Los cuerpos de cetona se forman en el cuerpo humano cuando las grasas se metabolizan cuando no hay suficiente glucosa para suministrar la energía del cuerpo. En individuos que tienen diabetes mal controlada cuando se descomponen grasas excesivas, estas cetonas pueden acumularse y la persona a menudo tiene una respiración afrutada como resultado.
Que es éster?
Definición:
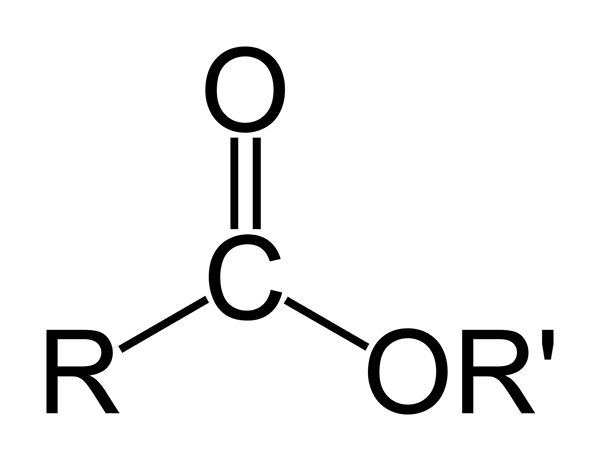
Un éster es una molécula que tiene un grupo de carbonilo y es una molécula en la que el hidroxilo ha sido reemplazado por un grupo que se conoce como un alcoxi (un átomo de oxígeno y un grupo alquilo).
Propiedades:
Los ésteres son moléculas que tienen polaridad (en otras palabras, tienen una carga) y, por lo tanto, reaccionan fácilmente con otras moléculas. Muchos ésteres pequeños son solubles en agua, pero el alcance de la solubilidad disminuye a medida que aumenta el tamaño de la molécula. Por lo tanto, los ésteres de cadena larga son insolubles en agua y forman parte de muchas moléculas lipídicas. Un éster es menos ácido que una cetona debido a la presencia del grupo alcoxi. También es menos reactivo que una molécula de cetona.
Formación:
Los ésteres se pueden formar a partir de alcoholes, ácidos carboxílicos y algunos de los ácidos inorgánicos como el ácido nítrico o el ácido fosfórico. El proceso en el que el ácido carboxílico reacciona con el agua en presencia de algún tipo de ácido en presencia de calor para formar un éster se conoce como esterificación.
Ejemplos y usos:
Hay muchos ejemplos de ésteres importantes, como por ejemplo, acetilcolina y ácido ascórbico (vitamina C). El acetato de etilo es un éster que ayuda a darle sabor a la cerveza. Algunos ésteres se utilizan para hacer aislamiento de alambre de PVC, ya que hace que el aislamiento sea flexible. Se pueden encontrar muchos ésteres de ácido tricarboxílico en el vino y ayudar a darle un olor específico al vino. Los ésteres se utilizan en la fabricación de muchas sustancias, incluidas Plexiglas y Mylar Film. Se utilizan diferentes ésteres para hacer tintes, solventes e incluso aditivos de gasolina.
Ocurrencia en la naturaleza:
Los ésteres de los ácidos grasos constituyen muchas de las diferentes grasas que ocurren en la naturaleza y a menudo se encuentran en las frutas. Las piñas y los plátanos tienen ésteres que le dan a las frutas un olor específico. Las ceras de las plantas también son un ejemplo de un éster que se encuentra en la naturaleza. Los ésteres de colesterol tomados a través de la dieta se utilizan para formar colesterol en animales, incluso en humanos.
Diferencia entre cetona y éster
Definición de cetona vs. Ester
Una cetona es una molécula que tiene un carbonilo unido a los carbonos. Un éster es una molécula que tiene un grupo de carbonilo y alcoxi unidos.
Acidez
Una cetona es una molécula más ácida. Un éster es una molécula menos ácida.
Reactividad
Las cetonas tienen más reactividad, mientras que los ésteres tienen menos reactividad.
Formación
La oxidación de los alcoholes e hidrocarburos puede producir una cetona, al igual que la hidratación de los alquinos. La reacción de esterificación en la que reaccionan el ácido carboxílico y el agua puede producir un éster.
Usos industriales
Las cetonas tienen muchos usos, incluidos los solventes como removeres de esmalte de uñas y removedores de pintura y laca, y pueden usarse para producir explosivos y en la industria de bronceado. Los ésteres también tienen varios usos que incluyen como solventes, tintes, como aditivos en la gasolina y para hacer películas de Mylar y plexiglás.
Ejemplos en humanos
Las cetonas se forman cuando las grasas se descomponen si no hay suficiente glucosa en el cuerpo para producir energía. Los ésteres se pueden tomar a través de la dieta y usarse para formar colesterol en humanos.
Tabla que comparó cetona y éster
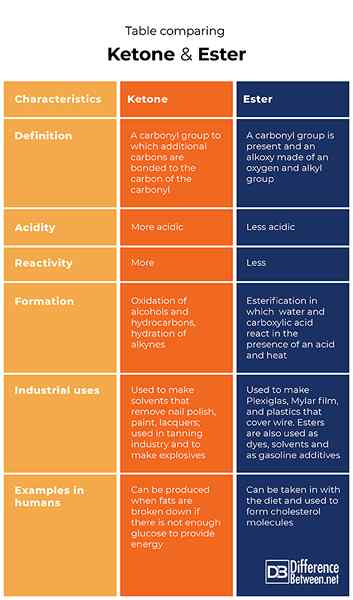
Resumen de cetona vs. Ester
- Las cetonas y los ésteres son moléculas que contienen un grupo carbonilo, pero hay diferentes átomos unidos al carbonilo en cada caso.
- Tanto las cetonas como los ésteres son moléculas que pueden usarse como solventes en ciertas situaciones.
- Las cetonas son más reactivas y ácidas que los ésteres.
- Los ésteres y las cetonas ocurren en organismos vivos.

