Butano vs. Metano

- 1493
- 224
- Pablo Carranza
Butano y metano son hidrocarburos de los mismos compuestos familiares químicos conocidos como alcanos. Son componentes del gas natural y la extracción de petróleo.
Cuadro comparativo
Diferencias - similitudes -| Butano | Metano | |
|---|---|---|
| número CAS | 106-97-8 Y | 74-82-8 años |
| Pubchem | 7843 | 297 |
| Químico | 7555 | 291 |
| Sonreír | CCCC | C |
| Pulgada | 1/C4H10/C1-3-4-2/H3-4H2,1-2H3 | 1/CH4/H1H4 |
| Fórmula molecular | C4H10 | CH4 |
| Masa molar | 58.12 g mol - 1 | dieciséis.042 g/mol |
| Apariencia | Gas sin color | Gas sin color |
| Densidad | 2.48 kg/m3, gas (15 ° C, 1 atm) 600 kg/m3, líquido (0 ° C, 1 atm) | 0.717 kg/m3, gas 415 kg/m3 líquido |
| Punto de fusion | −138.4 ° C (135.4 k) | -182.5 ° C, 91 K, -297 ° F |
| Punto de ebullición | −0.5 ° C (272.6 k) | -161.6 ° C, 112 K, -259 ° F |
| solubilidad en agua | 6.1 mg/100 ml (20 ° C) | 35 mg/L (17 ° C) |
| MSDS | MSD externos | MSD externos |
| NFPA 704 | 4 1 0 | 4 1 0 |
| punto de inflamabilidad | −60 ° C | -188 ° C |
| Límites explosivos | 1.8 - 8.4% | 5 - 15% |
| Alcanos relacionados | Propano; Pentano | Etano, propano |
| Compuestos relacionados | Isobutano; Ciclobutano | Metanol, clorometano, ácido fórmico, formaldehído, silano |
| Estructura y propiedades | n, εr, etc. | n, εr, etc. |
| Datos termodinámicos | Comportamiento de fase sólido, líquido, gas | Comportamiento de fase sólido, líquido, gas |
| Datos espectrales | UV, IR, RMN, MS | UV, IR, RMN, MS |
| Usos | El butano se usa en refrigeración, encendedores de cigarrillos, calentándose como GLP o gas licuado de petróleo. | El metano es una fuente de energía utilizada para fines de calentamiento. |
| Efectos dañinos | El butano puede causar asfixia y fibrilación ventricular. | El metano es un potente gas de efecto invernadero. Puede formar mezclas explosivas con aire. |
| Fuentes | Petróleo crudo, gas natural. | Campos de gas natural, producción de biogás, metano atmosférico, metano extra terrestres. |
Fórmula química y estructura molecular del metano vs butano
Butano es c4H10 mientras que el metano tiene la fórmula química - CH4. Por lo tanto, hay cuatro átomos de hidrógeno en una molécula de metano, mientras que hay diez átomos de hidrógeno en una molécula de butano. La molécula de metano forma una estructura tetraédrica, mientras que el butano es una estructura lineal.
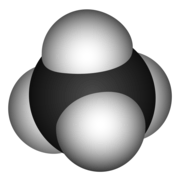 Molécula de metano: representación 3D
Molécula de metano: representación 3D 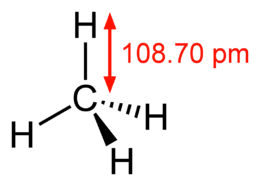 Molécula de metano: fórmula estructural determinada usando espectroscopía de microondas
Molécula de metano: fórmula estructural determinada usando espectroscopía de microondas 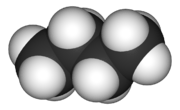 Molécula de butano: representación tridimensional
Molécula de butano: representación tridimensional 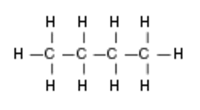 Molécula de butano - Fórmula química
Molécula de butano - Fórmula química Reacciones químicas de metano y butano
Butano reacciona con oxígeno para formar dióxido de carbono y vapor de agua. En condiciones de oxígeno limitado, el butano puede formar monóxido de carbono o carbono carbonizado. Reacciona con cloro para dar clorobutanos y otros derivados. Metano sufre combustión para dar formaldehído, monóxido de carbono y finalmente dióxido de carbono y vapor de agua. El proceso se conoce como pirólisis.
Facilitar el manejo
Tanto el metano como el butano son gases inodoro a temperaturas ambulantes. Butano Se puede licuar fácilmente, por lo tanto, se vende como combustible para acampar y cocinar. Se mezcla con propano y otros hidrocarburos de GLP, que se utiliza comercialmente para fines de calentamiento y cocción. Metano es difícil de transportar y es transportado por tuberías y transportistas de GNL.
A diferencia del metano, que es un gas terco en la presión y la temperatura normales, el butano se convierte en un líquido cuando se comprime. Esta propiedad se atribuye a los débiles enlaces del átomo de carbono central. Tan pronto como este gas licuado entra en contacto con el aire, reacciona con la fuente de encendido y se vuelve inflamable.
Isómeros
El butano exhibe isomerismo estructural a diferencia del metano y tiene dos isómeros, N-butano e iso-butano. El metano no exhibe isomerismo.
Usos de metano vs butano
El butano se usa en desodorantes, encendedores de cigarrillos, cilindros de gas para cocinar y calentar, propulsor en aerosoles y refrigerantes, etc. El metano también conocido como pantano o gas de pantano se usa para disparar estaciones de generación eléctrica, automóviles de energía, etc.
Fuentes
Metano se encuentra en humedales y océanos, atmósfera, fuentes humanas como el combustible quemado, la elevación del ganado, la fermentación de la materia orgánica, etc. Butano se puede obtener como subproducto durante la extracción de petróleo crudo y es un componente del gas natural.

