Diferencia entre el ácido acético y el ácido acético glacial
- 2111
- 134
- Carmen Arreola
¿Qué es el ácido acético??
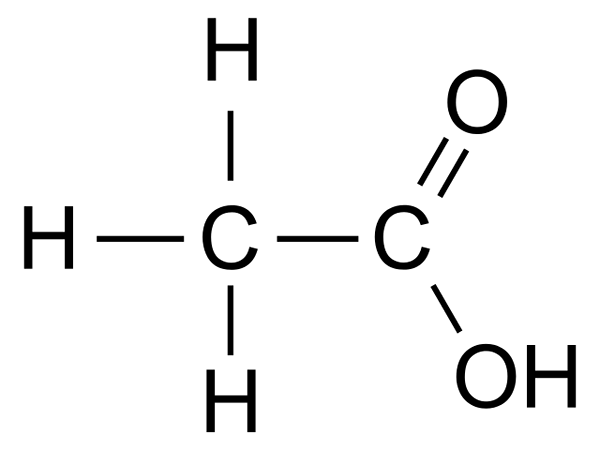
El ácido acético (CH3COOH) es uno de los ácidos carboxílicos más simples. Bajo la nomenclatura del sistema IUPAC, el nombre del ácido acético es el ácido etanoico.
El ácido acético se sintetiza en la descomposición y la fermentación acética. En la naturaleza, se encuentra en organismos vegetales y animales, tanto en estado libre como en forma de ésteres y otros derivados.
En el pasado, el ácido acético ha sido producido por la fermentación acética del alcohol etílico contenido en el vino. Por la acción de las enzimas bacterianas, el alcohol del vino es oxidado por el oxígeno del aire al ácido acético.
El método industrial para la producción de ácido acético es la oxidación catalítica directa de acetaldehído o butano. También puede producirse industrialmente por la carbonilación de metanol, catalizado por Rodium-Dodo.
El ácido acético es un líquido incoloro con un olor picante y un sabor agrio. Se disuelve muy bien en el agua. Debido a la mayor polaridad del enlace, los ácidos carboxílicos O-H forman enlaces de hidrógeno intermoleculares más fuertes que los alcoholes, lo que determina la solubilidad sin restricciones del ácido acético.
Las propiedades químicas del ácido acético están determinadas por su grupo funcional carboxilo y por el resto metilo. El ácido participa en reacciones químicas con la rotura de los enlaces en el grupo carboxilo.
El ácido acético muestra las propiedades químicas típicas de los ácidos orgánicos. En la solución de agua, el ácido acético se disocia según la ecuación:
Pez3COOH → CH3COO¯+ H
El grado de disociación electrolítica es significativamente menor que el de los ácidos inorgánicos fuertes, por lo que acético es un ácido débil. Reacciona con metales altamente electropositivos, óxidos básicos, hidróxidos básicos y sales de ácidos más débiles. Las sales obtenidas se llaman acetatos (etanoatos).
Las reacciones con óxidos, hidróxidos y sales rompen el enlace O-H en el grupo carboxilo.
La reacción de ácido acético con alcoholes en presencia de ácidos fuertes se llama esterificación, conduce a la producción de ésteres.
El ácido acético también participa en reacciones que afectan el grupo metilo - reacciones de sustitución en el resto hidrocarburos.
En forma de vinagre, las soluciones de ácido acético (5 a 18%) se utilizan en la industria alimentaria y en los hogares. El ácido acético se usa para la fijación de películas fotográficas, para eliminar los depósitos de calcio de grúas y calderas, para tratar una picadura de medusa, etc. También se usa como conservante para el ensilaje, ya que inhibe el crecimiento de bacterias y hongos.
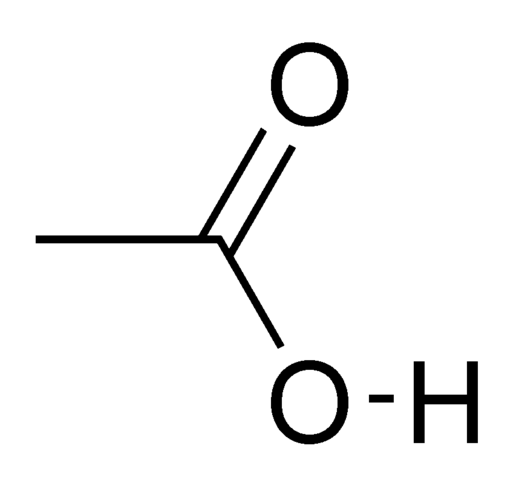
¿Qué es el ácido acético glacial??
El ácido acético puro y anhidro es un líquido higroscópico incoloro. A temperaturas inferiores a 16.7 ° C, forma cristales tipo hielo. Por eso se llama ácido acético glacial.
El ácido acético glacial hierve a alta temperatura (118 ° C). La razón de esto es la formación de enlaces de hidrógeno estables entre dos moléculas de ácido acético en forma de dímero cíclico. El punto de inflamabilidad es 39 ° C. La densidad a 25 ° C es 1.05 g/ml.
Durante siglos, los químicos han pensado que el ácido acético glacial y el ácido en el vinagre son dos sustancias diferentes.
El ácido acético glacial es corrosivo y sus vapores irritan los ojos y la nariz. En contacto con los ojos y la piel, puede provocar lesiones.
Al contacto del ácido acético con ácido acético glacial cristalizado, el ácido acético puro se une al cristal.
El ácido acético glacial es un gran solvente de base polar. A menudo se usa en la producción de:
- Ácido tereftálico;
- Propileno tereftalato;
- Alcanfor sintético;
- Anilina.
Diferencia entre el ácido acético y el ácido acético glacial
-
Definición
Ácido acético: El ácido acético es un ácido líquido incoloro (CH3COOH), con un olor picante y un sabor agrio.
Ácido acético glacial: El ácido acético puro y anhidro, formando cristales similares a hielo a temperaturas inferiores a 16.7 ° C, se llama ácido acético glacial.
-
Contenido de agua
Ácido acético: El ácido acético contiene agua.
Ácido acético glacial: El ácido acético glacial no contiene agua.
-
Cristalización
Ácido acético: El ácido acético no forma cristales.
Ácido acético glacial: A temperaturas inferiores a 16.7 ° C, el ácido acético glacial forma cristales tipo hielo.
-
Ocurrencia en la naturaleza
Ácido acético: En la naturaleza, el ácido acético se encuentra en organismos vegetales y animales.
Ácido acético glacial: El ácido acético puro y anhidro no ocurre en la naturaleza.
-
Producción
Ácido acético: El ácido acético se puede producir mediante fermentación acética, por oxidación catalítica directa de acetaldehído o butano, y por carbonilación de metanol, catalizado por Rodium-Dodo.
Ácido acético glacial: Al contacto del ácido acético con ácido acético glacial cristalizado, el ácido acético puro se une al cristal.
-
Uso
Ácido acético: El ácido acético se usa en la industria alimentaria y en los hogares (vinagre); para la fijación de películas fotográficas; para eliminar los depósitos de calcio de grúas y calderas; tratar una picadura de medusa, como conservante para el ensilaje, etc.
Ácido acético glacial: El ácido acético glacial se usa en la producción de ácido tereftálico, tereftalato de propileno, alcanfor sintético, anilina, etc.
-
Peligros
Ácido acético: El ácido acético no es peligroso en bajas concentraciones.
Ácido acético glacial: El ácido acético glacial es corrosivo y sus vapores irritan los ojos y la nariz. En contacto con los ojos y la piel, puede provocar lesiones.
Diferencia entre el ácido acético y el ácido acético glacial: tabla de comparación
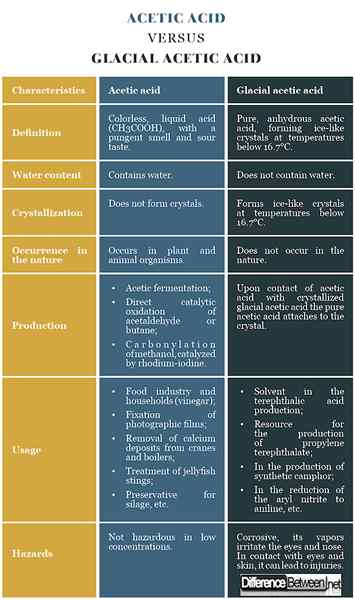
Resumen del ácido acético frente al ácido acético glacial
- El ácido acético es un ácido líquido incoloro (CH3COOH), con un olor picante y un sabor agrio.
- El ácido acético puro y anhidro, formando cristales similares a hielo a temperaturas inferiores a 16.7 ° C, se llama ácido acético glacial.
- El ácido acético contiene agua, mientras que el ácido acético glacial no.
- El ácido acético no forma cristales, mientras que a temperaturas inferiores a 16.7 ° C, el ácido acético glacial forma cristales tipo hielo.
- En la naturaleza, el ácido acético se encuentra en organismos vegetales y animales. El ácido acético puro y anhidro no ocurre en la naturaleza.
- El ácido acético se puede producir mediante fermentación acética, por oxidación catalítica directa de acetaldehído o butano, y por carbonilación de metanol, catalizado por Rodium-Dodo. Al contacto del ácido acético con ácido acético glacial cristalizado, el ácido acético puro se une al cristal.
- El ácido acético se usa en la industria alimentaria y en los hogares (vinagre); para la fijación de películas fotográficas; para eliminar los depósitos de calcio de grúas y calderas; tratar una picadura de medusa; Como conservante para el ensilaje, etc.
- El ácido acético glacial se usa en la producción de ácido tereftálico, tereftalato de propileno, alcanfor sintético, anilina, etc. etc.
- El ácido acético no es peligroso en bajas concentraciones. El ácido acético glacial es corrosivo y sus vapores irritan los ojos y la nariz. En contacto con los ojos y la piel, puede provocar lesiones.

