Diferencia entre acetona y agua
- 3192
- 444
- Sta. Magdalena Calvillo
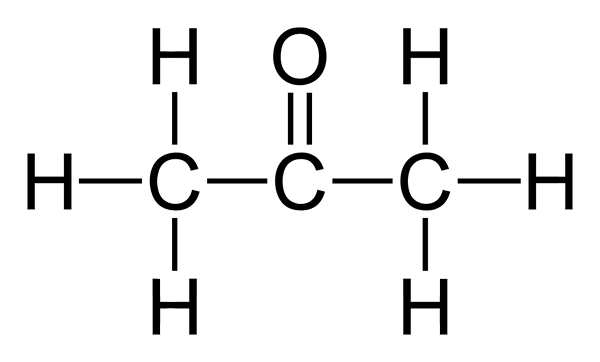
Que es acetona?
La acetona es la cetona más simple, también conocida como dimetil cetona o propanona. Su fórmula química es c3H6O. La acetona es un líquido incoloro y altamente inflamable con un olor específico.
La acetona se produce por la oxidación moderada de 2-propanol en presencia de un catalizador de cobre.
Se puede disolver en agua, etanol, éster y otros solventes.

El uso más común de la acetona es en el limpiador de esmaltes de uñas domésticos. También se utiliza en la producción de plásticos, tiras de películas, seda de acetato, caucho sintético, pólvora sin humo, algunos medicamentos, etc. Como un buen solvente para muchos compuestos orgánicos polares y no polares, se usa para limpiar las superficies contaminadas, como solvente para pinturas, barnices, varias reacciones sintéticas orgánicas, etc. Muchos de los plásticos se disuelven o hinchan en acetona.
La acetona ocurre en animales, plantas, escape del vehículo, incendios forestales, gases volcánicos, etc.
La acetona ocurre en el cuerpo humano en pequeñas cantidades. Después de la inanición prolongada o la dieta, el stock de carbohidratos en el cuerpo se agota y la grasa se descompone, lo que conduce a la producción de acetona. Como resultado, se produce la llamada "aliento de acetona". Los casos más graves dan como resultado cetoacidosis, que también es uno de los síntomas de la diabetes.
El vapor de acetona inhalado causa mareos e intoxicación. La acetona disuelve muy bien las grasas, por lo que causa piel seca y agrietada.
El peso molecular de la acetona es 58.08 g/mol. Sus vapores son dos veces más pesados que el aire. La densidad de la acetona relacionada con el agua es 0.8 (agua = 1). Es estable en las condiciones de almacenamiento recomendadas.
El punto de ebullición de Acetone es de 56 ° C, y su punto de fusión es -95 ° C. La auto-independiente ocurre a 465 ° C.
Que es el agua?
El agua es un compuesto inorgánico con una fórmula química H2O. A temperatura ambiente, es un líquido transparente, inodoro e incoloro.
En general, el agua se deriva de las fuentes naturales disponibles. Sin embargo, se desarrollan tecnologías alternativas de extracción de agua para áreas secas donde no hay fuentes de agua disponibles. Por ejemplo, en Marruecos se construye el sistema más grande del mundo para extraer agua del aire mediante condensación de niebla, cubriendo más de 600 metros cuadrados.
En Europa, aproximadamente el 42% del agua utilizada se usa en la agricultura, el 32% para las necesidades industriales, el 18% para la producción de energía y el 8% para fines nacionales. En los EE. UU., Alrededor del 70% del agua utilizada se usa en la agricultura, alrededor del 22% para las necesidades industriales y la producción de energía, y alrededor del 8%, para fines nacionales.
El agua cubre aproximadamente el 71% de la superficie de la tierra, principalmente en océanos y mares. Alrededor de 1.El 7% del agua ocurre como agua subterránea y 1.El 7% está congelado en glaciares y las casquillos de hielo.
En el cuerpo humano, hay alrededor del 70 - 75% del agua. La cantidad puede variar ligeramente y se observan las siguientes dependencias generales:
- Los bebés y los niños tienen un mayor porcentaje de agua que los adultos;
- Las mujeres tienen un porcentaje menor de agua que los hombres;
- Las personas con sobrepeso tienen un porcentaje menor de agua que el de peso normal.
Todos los procesos de la vida en el cuerpo humano están conectados con agua. El agua disuelve los nutrientes, elimina los productos de desecho. Proporciona metabolismo y es el entorno en el que tienen lugar todos los procesos bioquímicos.
El agua es uno de los compuestos menos tóxicos. Sin embargo, si se consume en una gran cantidad sin una intoxicación adecuada de agua de admisión de electrolitos.
El peso molecular del agua es de 18.02 g/mol. Sus vapores son más ligeros que el aire.
El punto de ebullición del agua es de 100 ° C, y su punto de fusión es 0 ° C. El agua es un compuesto estable. No es combustible y no se puede encender.
Diferencia entre acetona y agua
Definición
Acetona: Acetone es la cetona más simple, un líquido incoloro y altamente inflamable con un olor específico.
Agua: El agua es un compuesto inorgánico, un líquido transparente, inodoro e incoloro.
Fórmula química
Acetona: La fórmula química de la acetona es c3H6O.
Agua: La fórmula química del agua es h2O.
Producción
Acetona: La acetona se produce por la oxidación moderada de 2-propanol en presencia de un catalizador de cobre.
Agua: El agua se deriva de las fuentes naturales disponibles. Las tecnologías alternativas de extracción de agua se desarrollan para áreas secas donde no hay fuentes de agua disponibles.
Usar
Acetona: La acetona se usa en la producción de plásticos, tiras de películas, seda de acetato, caucho sintético, pólvora sin humo, algunos medicamentos, para limpiar superficies contaminadas, como solvente para pinturas, barnices, varias reacciones sintéticas orgánicas, etc.
Agua: El agua se utiliza en la agricultura, para las necesidades industriales, para la producción de energía y para fines nacionales.
Ocurrencia
Acetona: La acetona ocurre en animales, plantas, escape del vehículo, incendios forestales, gases volcánicos, etc.
Agua: El agua cubre aproximadamente el 71% de la superficie de la tierra, principalmente en océanos y mares. Alrededor de 1.El 7% del agua ocurre como agua subterránea y 1.El 7% está congelado en glaciares y las casquillos de hielo.
Presencia en el cuerpo humano
Acetona: Después de un hambre o dieta prolongada, se agota el stock de carbohidratos en el cuerpo, la grasa se descompone, lo que da como resultado la producción de acetona.
Agua: En el cuerpo humano, hay alrededor del 70 - 75% del agua.
Toxicidad
Acetona: El vapor de acetona inhalado causa mareos e intoxicación. La acetona disuelve muy bien las grasas, por lo que causa piel seca y agrietada.
Agua: El agua es uno de los compuestos menos tóxicos. Sin embargo, si se consume en una gran cantidad sin una intoxicación adecuada de agua de admisión de electrolitos.
Peso molecular
Acetona: El peso molecular de la acetona es 58.08 g/mol.
Agua: El peso molecular del agua es de 18.02 g/mol.
Punto de ebullición y fusión
Acetona: El punto de ebullición de Acetone es de 56 ° C, y su punto de fusión es -95 ° C.
Agua: El punto de ebullición del agua es de 100 ° C, y su punto de fusión es 0 ° C.
Auto-información
Acetona: La auto-independiente de Acetone ocurre a 465 ° C.
Agua: El agua no es combustible y no se puede encender.
Acetona vs. Agua: tabla de comparación
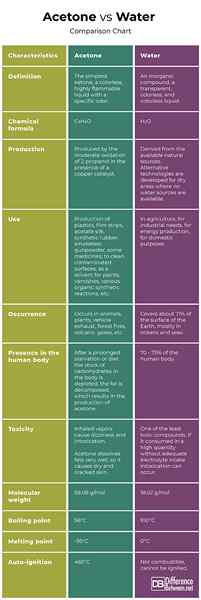
Resumen de acetona vs. Agua:
- Acetone es la cetona más simple, un líquido incoloro y altamente inflamable con un olor específico.
- El agua es un compuesto inorgánico, un líquido transparente, inodoro e incoloro.
- La fórmula química de la acetona es c3H6O y la fórmula química del agua es h2O.
- La acetona se produce por la oxidación moderada de 2-propanol en presencia de un catalizador de cobre. El agua se deriva de las fuentes naturales disponibles.
- La acetona se usa en la producción de plásticos, tiras de películas, seda de acetato, caucho sintético, pólvora sin humo, algunos medicamentos, para limpiar superficies contaminadas, como solvente para pinturas, barnices, varias reacciones sintéticas orgánicas, etc. El agua se utiliza en la agricultura, para las necesidades industriales, para la producción de energía y para fines nacionales.
- La acetona ocurre en animales, plantas, escape del vehículo, incendios forestales, gases volcánicos, etc. El agua cubre aproximadamente el 71% de la superficie de la tierra.
- Después de una inanición prolongada o una dieta, se agota el stock de carbohidratos en el cuerpo, la grasa se descompone, lo que resulta en la producción de acetona. En el cuerpo humano, hay alrededor del 70 - 75% del agua.
- La acetona es tóxica. El agua es uno de los compuestos menos tóxicos.
- El peso molecular de la acetona es 58.08 g/mol y el peso molecular del agua es 18.02 g/mol.
- El punto de ebullición de Acetone es de 56 ° C, y su punto de fusión es -95 ° C. El punto de ebullición del agua es de 100 ° C, y su punto de fusión es 0 ° C.
- La auto-independiente de Acetone ocurre a 465 ° C. El agua no es combustible y no se puede encender.

