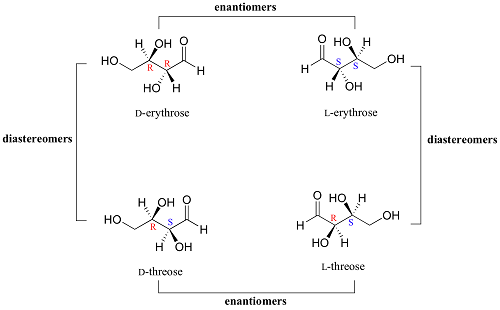
Diferencia entre enantiómeros y diastereómeros
- 1446
- 270
- María Elena Elizondo

El desafío de muchos estudiantes de química que estudian estereoquímica surge en la distinción entre enantiómeros y diastereomers. Estos son compuestos moleculares comunes con diferentes características a pesar de ser los estereoisómeros: compuestos con la misma fórmula molecular y estructural pero diferente orientación de átomos. Este artículo explicará la diferencia entre estos dos compuestos comunes para iluminarlo.
Primero, ¿qué es la estereoquímica?? Es el estudio de la disposición espacial de los átomos en un compuesto. Los enantiómeros y los diastereómeros son parte de los estereoisómeros: la misma fórmula estructural y molecular con diferentes disposiciones de los átomos en cada uno. Tenga en cuenta que los estereoisómeros pueden incluir muchos compuestos aparte de los enantiómeros y diastereomers. Estos pueden incluir los conformadores y los atropisómeros. Entre otros, nuestro enfoque está en diastereómeros y enantiómeros.
¿Qué son los enantiómeros??
Estas son las moléculas quirales que son imágenes espejo entre sí y no son superponibles. Una molécula quiral tiene una imagen que no es la misma que su imagen de espejo y generalmente se caracteriza por un centro de carbono con 4 átomos diferentes unidos. Estos átomos deben distinguirse químicamente para que una molécula sea calificada como quiral y, por lo tanto, un enantiómero. El carbón tetraédrico al que se unen los diferentes átomos se llama estereocentro. Vea la diferencia a continuación entre un carbono que se considera quiral y el que no califica.
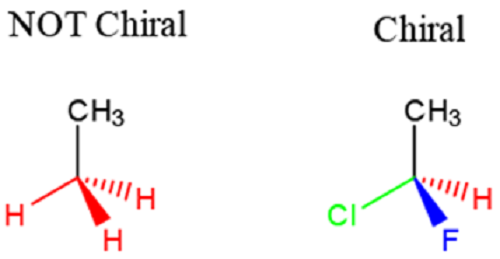
Fig. 1: Una ilustración de la molécula quiral y no quiral [1]
Debido a que hay una ligera diferencia en la disposición espacial de los átomos de las moléculas de enantiómeros, el Cahn-iningold-prelog Se estableció el sistema de nombres. Las dos moléculas tienen la misma fórmula y la estructuración de los átomos, por lo que para identificarlas tenemos que etiquetar una de la otra y la otra, dependiendo de la configuración en el sentido de las agujas del reloj de los átomos desde la masa atómica más baja hasta la masa atómica más alta. Por ejemplo, un carbón estereocentro con bromo, cloro, flúor e hidrógeno unido respectivamente en sentido horario, a la molécula se le asignará una R, y si es antihorario, a la molécula se le asignará una S porque el bromo tiene la masa atómica más alta y hidrógeno el más bajo.
La disposición de estos átomos en realidad ayuda a determinar las propiedades de la molécula. Considere las estructuras de bromocloroflurometano a continuación:
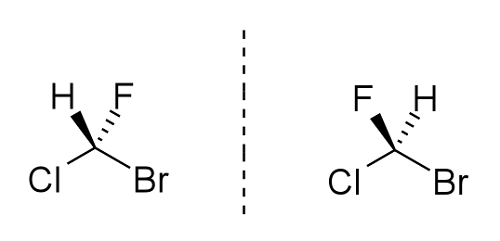
Es evidente que la orientación del hidrógeno y el flúor es diferente pero del mismo compuesto molecular. No importa cuántas veces pueda rotar la molécula derecha, nunca tendrá la misma orientación que la molécula izquierda. Si, por ejemplo, intenta intercambiar el flúor y el hidrógeno alrededor, el bromo y el cloro también cambiarán sus posiciones. Esto explica claramente los conceptos de imágenes no superpositables y de espejo de enantiómeros.
Para nombrar a las moléculas, al quiral (estereocentro) se le asigna una letra s o r. Los componentes, por lo tanto, el fluorino, el cloro, el bromo, están marcados de masa atómica alta a baja asignando 1, 2, 3. El bromo es el más alto, por lo que se asigna 1, el cloro 2 y el flúor 3. Si la rotación es de 1 a 3 en sentido horario, entonces el centro quiral se designa r, si es contrario, entonces s. Así es como funciona el sistema Cahn-Ondold-Prelogs para distinguir los enantiómeros entre sí. Se vuelve simple cuando trabajamos con un centro quiral con 4 sustituyentes únicos adjuntos. Un enantiómero puede tener más de 2 centros quirales.
Las moléculas de los enantiómeros son distintas en términos de disposición espacial de los átomos, pero tienen las mismas propiedades químicas y físicas. Dicho esto, tienen los mismos puntos de fusión, puntos de ebullición y muchas más propiedades. Sus fuerzas intermoleculares son idénticas; esto explica las mismas propiedades. Pero sus propiedades ópticas son diferentes porque rompen la luz polarizada en direcciones opuestas, aunque en cantidades iguales. Esta diferencia en las propiedades ópticas distingue las moléculas enantiómicas.
¿Qué son los diastereómeros??
Estos son los compuestos estereoisómeros con moléculas que no son imágenes espejo entre sí y que no son superponibles. El ejemplo perfecto de diastereómeros es cuando miras las estructuras de los isómeros cis y trans. Ver las estructuras cis-2-butene y trans-2-buteno a continuación:
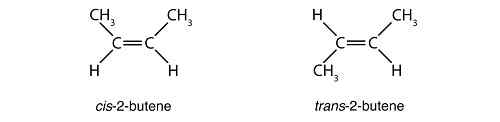
Los compuestos son idénticos, pero la disposición es diferente, y no son las imágenes del espejo entre sí. Cuando el CH3 están del mismo lado, el compuesto es cis y cuando el otro se intercambia con el átomo de hidrógeno, nombramos el compuesto trans. Pero el cis y trans Las estructuras no son los únicos ejemplos de diastereómeros. Hay muchas de estas moléculas, siempre y cuando demuestren las disposiciones espaciales de los átomos que no son imágenes espejo entre sí, y que no son sumpersables.
A diferencia de los enantiómeros, los diastereómeros tienen diferentes propiedades físicas y químicas. Los diastereómeros tienen dos estereocentros por los cuales la otra estructura molecular puede imitar las configuraciones de enantiómeros, mientras que el otro tiene la misma configuración. Esto es lo que los distingue de los enantiómeros porque no hay forma de que estas estructuras puedan ser imágenes espejo entre sí.
La siguiente tabla resaltará las diferencias clave entre los enantiómeros y los diastereómeros en pocas palabras:
| Enantiómeros | Diastereómeros |
| Son imágenes espejo entre sí y no son superposibles | No son imágenes espejo entre sí y no son superposibles |
| Sus estructuras moleculares a menudo diseñadas con R y S para distinguirlas. | Una molécula imita las estructuras de enantiómeros, mientras que la otra tiene la misma configuración. Por lo tanto, no hay necesidad de usar el nombre para diferenciarlos. |
| Tener las mismas propiedades químicas y físicas pero diferentes propiedades ópticas | Tener diferentes propiedades químicas y físicas |
| Tener uno o más estereocentro | Tener dos estereocentros |
| Todos los enantiómeros poseen actividad óptica activa, aunque giran la luz en direcciones opuestas. Aquellos que giran la luz en sentido antihorario se conocen como levorotario, y los que giran en sentido horario se conocen como dextrorotario. Pero cuando el otro tiene las mismas cantidades de rotación dextrorotería y levorotaria, se considera una mezcla de raza y, por lo tanto, ópticamente inactiva. | No todos los diastereómeros poseen actividad óptica |
Envolver!
Los enantiómeros y los diastereómeros son estereoisómeros con la misma fórmula molecular y estructural pero una disposición/configuración diferente de los átomos que hacen sus estructuras. Hemos visto que las moléculas enantiómeras son las imágenes espejo entre sí y los diastereómeros no son imágenes espejo. Ambas moléculas no son sumpersables.
Los enantiómeros tienen las mismas propiedades químicas y físicas, pero difieren en las propiedades ópticas porque algunos giran la luz polarizada en direcciones opuestas. Por otro lado, no todos los diastereómeros tienen la actividad óptica.
También hemos visto cómo se desarrollan el nombre de las estructuras de los enantiómeros con el sistema de nomenclatura R y S asignado en función de la masa atómica de los sustituyentes unidos en el centro quiral. En los diastereómeros, solo una estructura tiene la configuración R y S mientras que la otra tiene las mismas configuraciones. Esto es lo que los distingue de las imágenes de espejo enantiómero.

