Diferencia entre oxidación y combustión
- 982
- 92
- Juan Carlos Rodrígez
 Oxidación vs combustión
Oxidación vs combustión
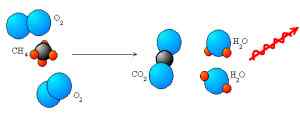
Hemos oído hablar del proceso de combustión y oxidación en nuestra escuela. Pero solo unos pocos saben sobre las principales diferencias entre ellos. En combustión, los compuestos orgánicos se queman por completo y se oxidan al CO2 y al agua. El proceso necesita oxígeno para ocurrir. Sin embargo, en la oxidación, se agrega oxígeno al compuesto. En caso de oxidar el elemento, podemos decir que se ha perdido un ion de carga negativa o se pierde un átomo del elemento.
Cada vez que la combustión se lleva a cabo la oxidación es el resultado final, pero no es lo mismo para la oxidación. La combustión se acompaña de reacciones exotérmicas que ocurren después de una serie de reacciones químicas complejas. Implica un oxidante que se requiere para catapultar el experimento. El calor y la luz también se producen durante la reacción. Por otro lado, en oxidación, se gana oxígeno y las moléculas de hidrógeno o los electrones se pierden así, dando al elemento o al compuesto una forma oxidada.
Lo que sucede en la combustión? En este proceso, el compuesto reacciona con el elemento que actúa como un elemento oxidante (por ejemplo, oxígeno o flúor). La sustancia final obtenida consiste en compuestos que también tienen el elemento oxidante como parte de su química. ¿Cuál es el procedimiento de oxidación?? En oxidación, el estado de oxidación del compuesto es cambiado por dos procesos:
Proceso redox: por ejemplo, la oxidación del carbono al CO2.
Reducción del elemento de carbono para obtener CH4, también conocido como metano mediante la ayuda de hidrógeno.
Esto también puede estar representado por el ejemplo de oxidación de azúcar que tiene lugar dentro del cuerpo humano. Este proceso implica una serie de procesos muy complejos que incluye transferencias de electrones dentro de la estructura celular.
Puede haber diferentes tipos de procesos de combustión como combustión rápida, combustión completa y combustión incompleta. Podemos definir la oxidación como un proceso en el que el oxígeno reacciona con las sustancias que vienen en su contacto y forman sustancias que tienen diferentes propiedades. Por ejemplo, el hierro o el Fe se convierten en Fe3o4 cuando el oxígeno reacciona con él. Esto también se denomina oxidad que ocurre en nuestra vida cotidiana. La oxidación también puede tener lugar en el caso de los organismos vivos.
La combustión tiene lugar en los combustibles líquidos que quemas en tus vehículos. Este proceso tiene lugar en una atmósfera donde el oxígeno está disponible y toda la reacción tiene lugar en una fase gaseosa.
Resumen:
1. En el proceso de combustión, los compuestos orgánicos se oxidan en las moléculas de carbono y H2O. El proceso requiere participación de oxígeno. Mientras que en la oxidación, se pierde un ion mediante la adición de oxígeno.
2. En la combustión, la oxidación es el proceso final, pero lo mismo no es cierto para el proceso de oxidación.
3. En la combustión se producen calor y luz, pero esto no es lo mismo con la oxidación.

